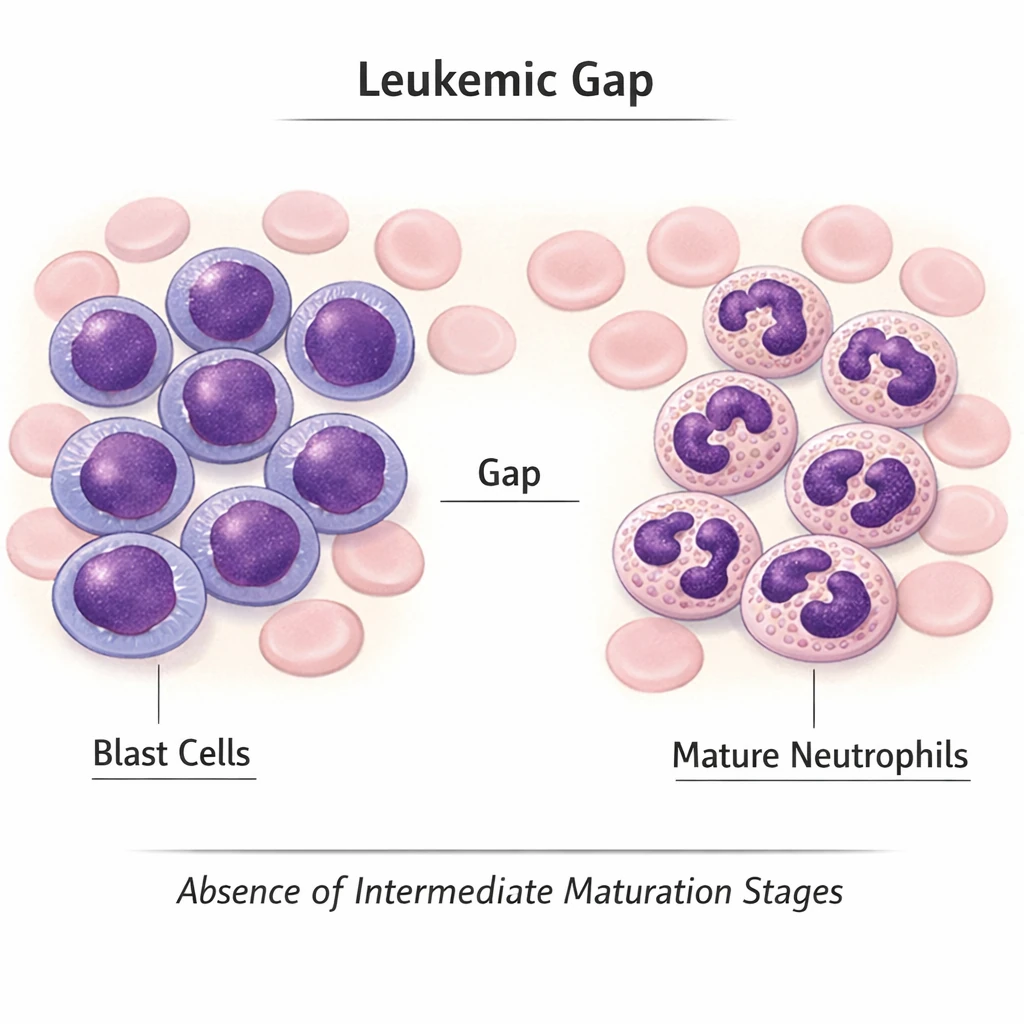
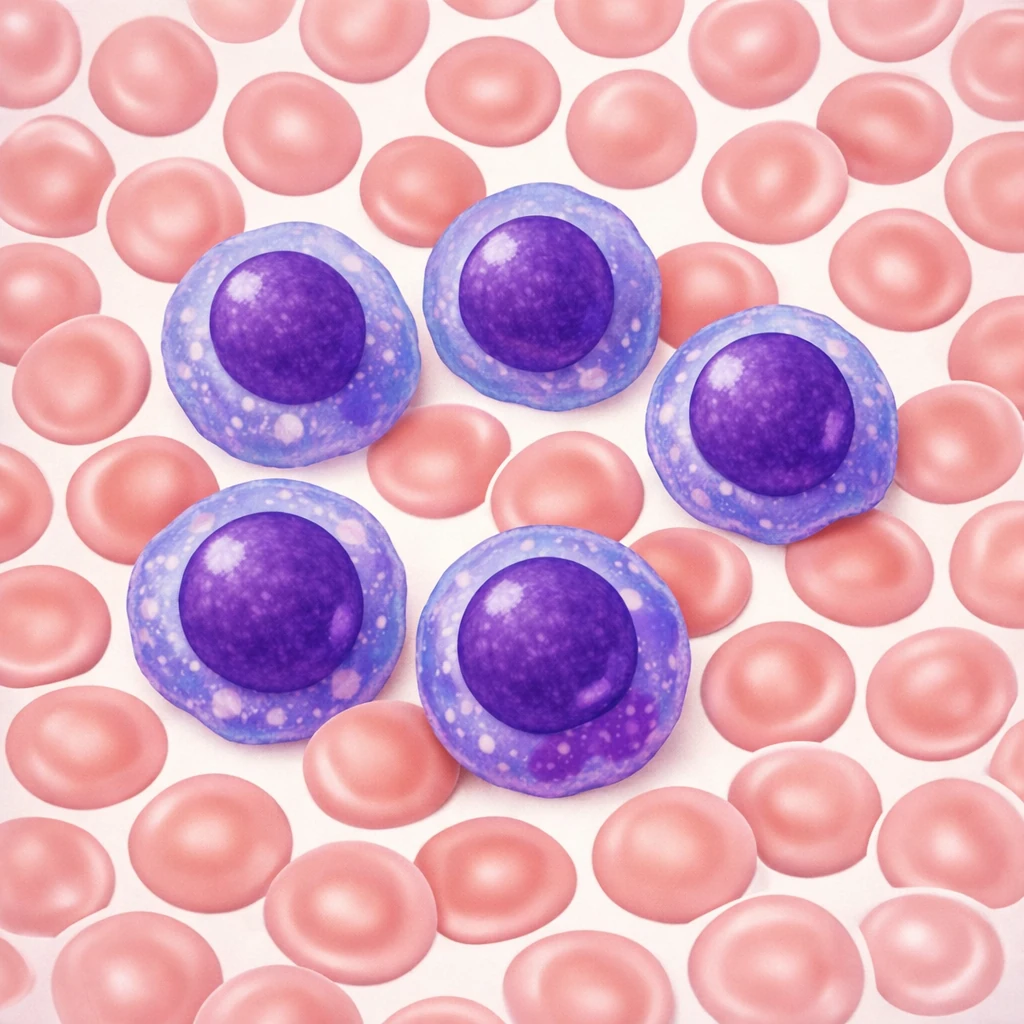
آنتیبادی ضد GAD یا Anti‑GAD (Glutamic Acid Decarboxylase Antibody) یکی از نشانگرهای مهم خودایمنی است که میتواند در دو بستر کاملاً متفاوت ظاهر شود: دیابت نوع یک و سندرم استیفمن (Stiff‑Person Syndrome – SPS). در اولی، هدف حمله سلولهای β پانکراس است و در دومی، گیرندههای عصبی مهاری (GABAergic) در سیستم عصبی مرکزی مورد تهاجم قرار میگیرند. شناخت این آنتیبادی نهتنها به افزایش دقت تشخیص کمک میکند، بلکه در درک پیوند میان خودایمنی متابولیک و نورولوژیک نقشی کلیدی دارد.
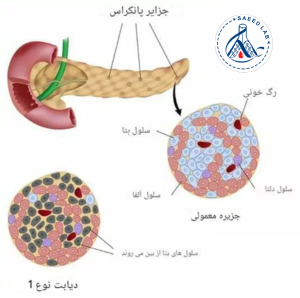
Anti‑GAD چیست و چگونه عمل میکند؟
GAD آنزیمی است که مسئول تبدیل گلوتامات به GABA (انتقالدهنده عصبی مهارکننده) است. دو ایزوفرم اصلی آن GAD‑۶۵ و GAD‑۶۷ در سلولهای عصبی و سلولهای β پانکراس وجود دارند. زمانی که سیستم ایمنی به اشتباه علیه این پروتئین واکنش نشان میدهد، آنتیبادیهای ضد GAD تشکیل میشوند.
مکانیسم اثر آنتیبادیها:
– مهار فعالیت آنزیم GAD و کاهش میزان GABA در سیناپسهای عصبی
– اختلال در عملکرد سلولهای β پانکراس و کاهش ترشح انسولین
– تحریک مسیرهای التهابی T‑cell و بروز آسیب مزمن عصبی یا متابولیک
نقش Anti‑GAD در دیابت نوع یک (T1DM)
دیابت نوع یک اساساً یک بیماری خودایمنی است که در آن سلولهای β پانکراس تخریب میشوند. حضور Anti‑GAD یکی از شاخصهای تشخیص اولیه است و معمولاً پیش از بروز علائم بالینی میتواند نشان دهد که روند ایمنی در حال فعال شدن است.
ویژگیهای کلینیکی مهم:
– شایعترین آنتیبادی در دیابت خودایمن بزرگسالان (LADA)
– پایدارترین مارکر سرولوژیک در مراحل مزمن بیماری
– مثبت بودن آن حتی پس از چند سال از شروع بیماری
– همراهی گاهبهگاه با سایر آنتیبادیها مانند Anti‑IA2 و Anti‑ZnT8
کاربردهای بالینی تست Anti‑GAD در دیابت:
– افتراق دیابت نوع یک از نوع دو در بیماران بزرگسال
– پیشبینی بروز دیابت در بستگان درجه یک بیماران مبتلا
– تعیین نیاز به درمان انسولینی در موارد LADA
ارتباط Anti‑GAD با سندرم استیفمن (SPS)
سندرم استیفمن یک اختلال عصبی خودایمن نادر است که با سفتی عضلات تنه، اسپاسم دردناک و افزایش تحریکپذیری عصبی همراه است. در ۷۰–۸۰٪ بیماران SPS، آنتیGAD در تیتر بسیار بالا یافت میشود (اغلب >10,000 IU/mL) که بیانگر فعال شدن خودایمنی علیه سلولهای تولید GABA در CNS است.
ویژگیهای بالینی سندرم استیفمن همراه با Anti‑GAD:
– سفتی تدریجی عضلات محوری و پشت
– تشدید اسپاسمها در اثر استرس یا محرکهای صوتی
– اغلب وجود همزمان دیابت نوع یک یا سایر بیماریهای خودایمنی
– پاسخ نسبی به درمان با IVIg و بنزودیازپینها
نقاط اشتراک ایمنی بین دیابت نوع یک و SPS
دیابت نوع یک و SPS هر دو نتیجه بروز خودایمنی علیه پروتئینهای مشترک هستند. تهاجم به GAD‑۶۵ در سلولهای β پانکراس و نورونهای مهاری، نمونهای از “تقلید مولکولی” بین بافتهای متابولیک و عصبی است.
وجه مشترکهای کلیدی:
– حضور آنتیGAD در هر دو بیماری
– فعال شدن سلولهای T و مسیر CD4+ در پاسخ ایمنی
– زمینه ژنتیکی مشترک HLA‑DR3 و DR4
– احتمال افزایش خطر سایر بیماریهای خودایمن مانند تیروئیدیت و سلیاک
تست Anti‑GAD؛ نحوه انجام و تفسیر
روشهای آزمایشگاهی:
– معمولاً با روش ELISA یا Radioimmunoassay انجام میشود.
– نمونه مورد نیاز سرم است و ترجیحاً در حالت پایدار متابولیک گرفته میشود.
تفسیر دقیق نتایج:
– تیتر پایین (≤۲۰۰ IU/mL) بیشتر با دیابت نوع یک همراه است.
– تیتر بسیار بالا (>1000 IU/mL) احتمال درگیری عصبی یا SPS را مطرح میکند.
– وجود همزمان سایر آنتیبادیهای خودایمن، شدت و گستره بیماری را تعیین میکند.
درمان و پیامدهای بالینی
در دیابت نوع یک، درمان بر پایه جایگزینی انسولین و کنترل خودایمنی غیرمستقیم است. اما در SPS، رویکرد درمانی فعالتر و مبتنی بر سرکوب ایمنی است.
رویکرد درمانی بر اساس وضعیت بیماران با Anti‑GAD مثبت:
– دیابت: انسولین، کنترل دقیق HbA1c، و بررسی سایر اختلالات ایمنی همراه
– SP** IVIg، پلاسماآفرز، کورتون یا ریتوکسیماب بر اساس شدت علائم
– در هر دو: اصلاح سبک زندگی، پایش عصبی و بررسی تیتر آنتیGAD بهصورت دورهای
پرسشهای متداول (FAQ)
۱. آیا Anti‑GAD مثبت همیشه نشانه بیماری است؟
خیر، تیتر پایین آن گاهی در افراد سالم یا حامل زمینه ژنتیکی دیابت مشاهده میشود؛ اما تیتر بالا معمولاً نیازمند بررسی بالینی و نورولوژیک است.
۲. آیا وجود Anti‑GAD در دیابت و SPS با هم میتواند درمان را دشوار کند؟
بله، همزمانی آن نشاندهنده درگیری گستردهتر سیستم ایمنی است و نیاز به رویکرد چندتخصصی دارد.
۳. آیا Anti‑GAD قابل درمان یا حذف از بدن است؟
خیر، اما با کنترل بیماری زمینهای و درمان ایمنی، تیتر آن ممکن است کاهش یابد یا پایدار بماند بدون پیشرفت آسیب بیشتر.
جمعبندی
Anti‑GAD یک آنتیبادی کلیدی در تلاقی میان اتوایمونیتی متابولیک و عصبی است. در حالی که در دیابت نوع یک نقش تشخیصی و در SPS نقش پاتولوژیک دارد، شناسایی دقیق آن میتواند در پیشگیری، درمان زودهنگام و ارائه مراقبت شخصیسازیشده کمک شایانی کند. توجه به تیتر، زمینه بالینی و سایر مارکرهای همراه، پایه تصمیمگیری بالینی دقیق در این بیماران است.
منابع :
– [MedlinePlus – Type ۱ Diabetes Overview]
– [Cleveland Clinic – Stiff‑Person Syndrome Information]
No. 97
۰۴/۰۸